Uno de los mayores dolores de cabeza en química es intentar imaginar figuras tridimensionales mirando un libro plano. Te dicen que el metano es un “tetraedro”, pero en el papel parece una cruz plana.
Hoy vamos a resolver eso. Vamos a utilizar el Visualizador Online para aplicar la Teoría RPECV (Repulsión de Pares de Electrones de la Capa de Valencia) y ver cómo los átomos se organizan realmente en el espacio.
¿Qué es la Teoría RPECV?
Básicamente, los electrones se odian entre sí. Como tienen carga negativa, los pares de electrones que forman enlaces (o los pares libres) intentan alejarse lo máximo posible unos de otros. Esta repulsión es la que da forma a la molécula.
Para entenderlo, no basta con leerlo. Tienes que verlo.
👉 ENTRA AL VISUALIZADOR ONLINE AQUÍ
(Instrucciones: Abre la herramienta, toca la Lupa 🔍 y busca las moléculas que mencionamos abajo).
1. Geometría Lineal (180∘)
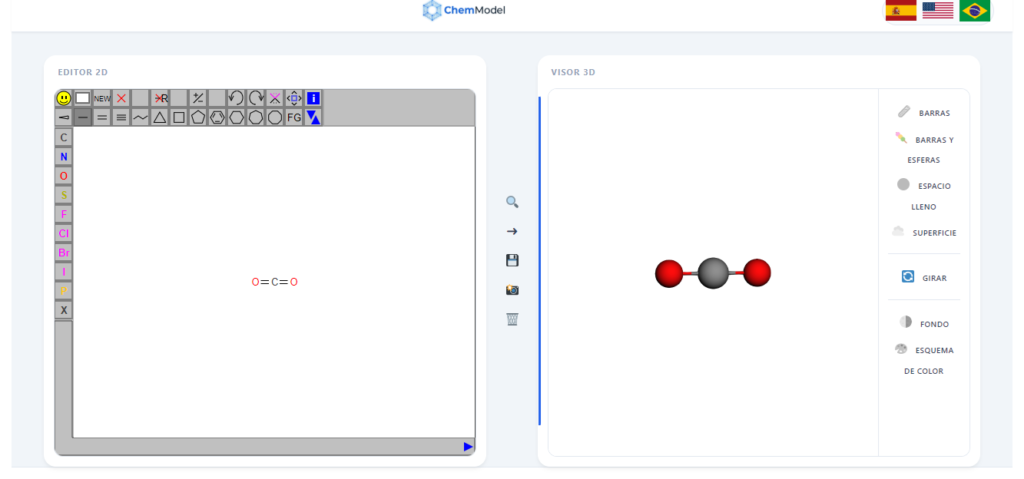
El ejemplo clásico es el Dióxido de Carbono (CO2).
- En el Visualizador: Busca “Carbon Dioxide” o “Dioxido de carbono”.
- Qué observar: Verás que los tres átomos están alineados perfectamente. Los electrones de los dobles enlaces se empujan hasta quedar en lados opuestos.
- Estilo recomendado: Usa el modo “Barras y Esferas” para ver claramente la alineación.
2. Geometría Trigonal Plana (120∘)
Busca el Trifluoruro de Boro (BF3) o dibújalo en el editor 2D.
- Qué observar: Imagina un triángulo equilátero. El átomo de Boro está en el centro y los tres Flúor en las esquinas, todos en el mismo plano plano.
3. Geometría Tetraédrica (109.5∘)
Aquí es donde el dibujo en papel falla. Busca el Metano (CH4).
- El error del papel: En tu cuaderno, el metano parece una cruz de 90 grados.
- La realidad 3D: En nuestro visualizador, verás que es un trípode. Gira la molécula con el botón “Girar” o con el mouse. No importa cómo la mires, siempre hay átomos apuntando hacia ti y hacia atrás. Esa es la magia del tetraedro.
4. El Efecto de los Pares Libres: Agua (H2O)
Busca “Agua”. Aunque el oxígeno tiene 4 zonas de electrones (como el metano), dos de ellas son pares solitarios (invisibles pero poderosos). Estos pares empujan a los hidrógenos hacia abajo, cerrando el ángulo de 109.5∘ a unos 104.5∘.
- Prueba esto: Cambia el estilo a “Espacio Lleno”. Verás cómo el oxígeno “ocupa” mucho espacio por arriba, aplastando a los hidrógenos.
Reto para tu Examen:
Usa el Visualizador Online para predecir y comprobar la geometría de estas moléculas:
- Amoníaco (NH3): ¿Es plana o piramidal?
- Hexafluoruro de Azufre (SF6): Una estructura octaédrica impresionante.
La química no es plana. Dejar de memorizar ángulos y empezar a visualizarlos es la clave para dominar la RPECV. ¡Usa nuestra herramienta para hacer tus tareas y entender la estructura real del universo a escala atómica!